Tabela Periódica dos Espectros de Emissão
Que tabela periódica é esta?
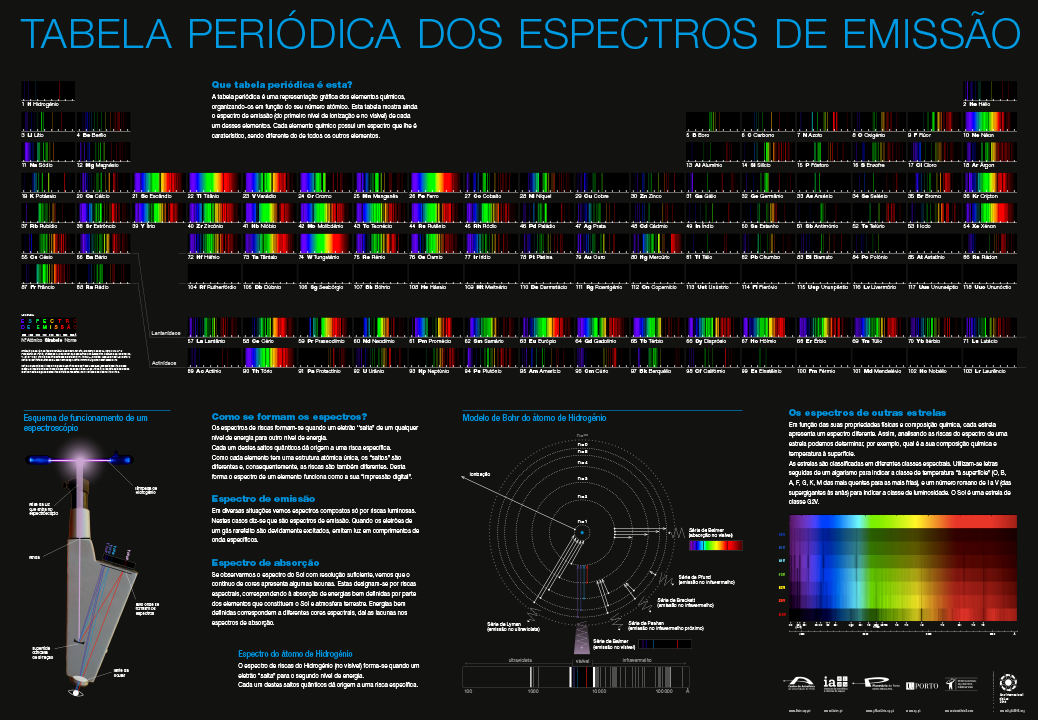
A tabela periódica é uma representação gráfica dos elementos químicos, organizando-os em função do seu número atómico (número de protões no núcleo desse elemento). Esta tabela mostra ainda, para cada elemento, o seu espectro de emissão – gama de radiação emitida – do primeiro nível de ionização e no visível.
Cada elemento químico possui um espectro que lhe é caraterístico, sendo, por isso, como que uma “impressão digital”.
Como se formam os espectros?
Os espectros de riscas formam-se quando um eletrão transita de um nível de energia, para outro. Nesse processo, emite. ou absorve energia.
Cada uma destas transições eletrónicas dá origem a uma risca específica. Assim, como cada elemento tem uma estrutura atómica única, as transições eletrónicas são diferentes. Como consequência, os fotões emitidos ou absorvidos terão diferentes energias, originado riscas em zonas específicas do espectro. Desta forma, o espectro de um elemento funciona como a sua “impressão digital”.
Espectro de emissão
Em diversas situações vemos espectros formados só por riscas coloridas. Esses são designados espectros de emissão e resultam das radiações emitidas pelas substâncias.
Espectro de absorção
Se algumas radiações forem absorvidas, no trajeto entre uma fonte luminosa (por exemplo, uma estrela) e a entrada de um detetor, obtem-se um espectro de absorção. Este é assim formado por riscas negras que correspondem, exatamente, às radiações que foram absorvidas (por exemplo, pela atmosfera da estrela).
Espectro do átomo de hidrogénio
Fazendo uma descarga elétrica num gás composto exclusivamente por hidrogénio, podemos excitar os átomos desse gás. Contudo, esses átomos perdem rapidamente esse excesso de energia e ao fazê-lo, emitem radiação (ultravioleta, visível ou infravermelha). Podemos, desta forma, registar o espectro do átomo de hidrogénio.
CONSULTAR
—
A Tabela Periódica dos Espectros de Emissão, foi criada no âmbito do Ano Internacional da Luz (2015), uma nova versão em formato digital foi produzida âmbito do Ano Internacional da Tabela Periódica (2019).
Cartaz impresso 100 x 70 cm, em português, disponível para as escolas que realizem a oficina Impressão Digital dos Astros do Planetário do Porto – CVV.
Disponibilizámos para download imagens com boa resolução para monitores ou projeção: aqui (em PT) e aqui (em ENG).

 Rua das Estrelas, 4150-762 Porto
Rua das Estrelas, 4150-762 Porto
T. +351 226 089 800 (chamada para a rede fixa nacional)
geral@planetario.up.pt
Mapa e como chegar





